
Lekooporność – wróg farmakoterapii
Mimo że na przestrzeni czasów rozwój nauk medycznych pozwolił opanować wiele chorób, a nawet epidemii, wciąż jednak ogromny jest obszar poszukiwań skutecznych metod terapii. Przyczyną tego zjawiska jest problem lekooporności, czyli oporności komórek bakteryjnych bądź nowotworowych na działanie jednego lub większej liczby chemioterapeutyków. Nową nadzieją na rozwiązanie tego problemu są substancje hamujące mechanizmy lekooporności, nad którymi pracują m.in. naukowcy z Wydziału Farmaceutycznego UJ CM.
Zgodnie z szacunkami Światowej Organizacji Zdrowia (WHO), co roku z powodu chorób zakaźnych umiera na świecie ponad piętnaście milionów ludzi. Lekarze są bezsilni wobec infekcji wywoływanych przez bakterie oporne na działanie antybiotyków. Wzrost oporności na antybiotyki, jak przestrzegają epidemiolodzy, grozi powrotem „ery przedantybiotykowej", kiedy to zgonem kończyło się nawet najprostsze zapalenie płuc. Już dziś z powodu lekoopornych bakterii w Polsce umiera rocznie około 20–30 tysięcy osób.
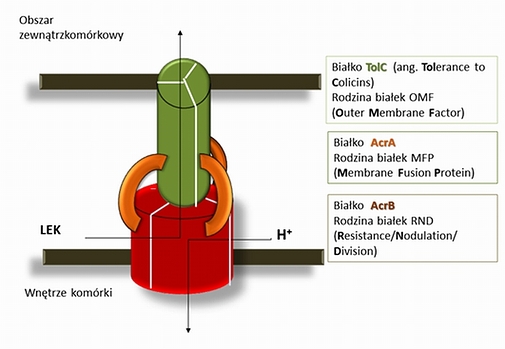
Trójdzielna białkowa pompa lekooporności AcrA/AcrB/TolC charakterystyczna dla niektórych bakterii Gram-ujemnych (E. coli, E. aerogenes)
Lekooporność – wróg farmakoterapii
Oporność komórek patogennych na większą ilość leków, zwana wielolekoopornością, czyli MDR (ang. Multi Drug Resistant), jest zespołem mechanizmów obronnych komórek. Wpływa ona na obniżenie skuteczności działania leku, który ma na celu zahamowanie przyczyn, objawów oraz zapobieganie rozwojowi choroby poprzez modyfikację procesów fizjologicznych patogennych komórek. Lekooporność stanowi przeszkodę w skutecznej terapii zarówno chorób o podłożu bakteryjnym, grzybiczym, jak i nowotworów.
Wyróżniamy dwa typy lekooporności: oporność pierwotną i oporność nabytą. Oporność pierwotna nie zależy od wcześniejszego kontaktu z lekiem, jest cechą wrodzoną mikrobów. Przykładem tego typu oporności są wszystkie szczepy pałeczki ropy błękitnej Pseudomonas aeruginosa, które są odporne na większość antybiotyków ze względu na fakt, że posiadają złożoną ścianę komórkową, która ogranicza penetrację leków do wnętrza komórki. Oporność nabyta pojawia się natomiast już po rozpoczęciu terapii. Odpowiadają za nią dwa podstawowe mechanizmy: przekazywanie genów oporności pomiędzy bakteriami oraz mutacje. W nabywaniu genów oporności najczęściej pośredniczą plazmidy, specyficzne cząsteczki DNA występujące w komórce, z kolei oporność mutacyjna wynika z mutacji chromosomalnej (zmiany budowy jednego lub więcej chromosomów), która czyni bakterię niezdolną do oddziaływań z lekiem przeciwbakteryjnym.
Pompy białkowe na straży patogennych komórek
Jednym z podstawowych mechanizmów lekooporności drobnoustrojów chorobotwórczych i komórek nowotworowych są białkowe pompy wyrzutu leków, które pełnią rolę „strażników" kontrolujących substancje wnikające do wnętrza komórki. Reprezentują one różne rodziny białek transportujących i posiadają zdolność usuwania z wnętrza komórek chemioterapeutyków, antybiotyków, detergentów, barwników oraz rozpuszczalników organicznych. Błonowe białka transportujące mogą przyczyniać się do zwiększenia oporności pierwotnej i nabytej, dlatego też są one potencjalnym celem w tworzeniu nowej generacji leków przeciwbakteryjnych, których projektowanie znacznie ułatwia znajomość struktury tych białek. Ich badanie nie jest łatwym zadaniem, m.in. ze względu na ich niski poziom ekspresji – stanowią one mniej niż 0,1% masy wszystkich białek komórkowych. Stąd na przeszło ośmiu tysiącach zidentyfikowanych eksperymentalnie struktur białek bakteryjnych słabo rozpuszczalne białka błonowe stanowią mniej niż sto.
Nadprodukcja białkowych pomp wyrzutu leków, której przyczyną mogą być mutacje, jest główną przyczyną uodporniania się szczepów bakteryjnych na antybiotyki i inne środki lecznicze. Trójdzielne pompy RND/MFP/ /OMF stanowią podstawowy mechanizm lekooporności wśród najbardziej agresywnych bakterii Gram-ujemnych.
Jedną z najlepiej poznanych do tej pory pomp wyrzutu leków jest trójskładnikowa pompa AcrA/AcrB/ TolC, występująca u bakterii Escherichia coli, oraz Pseudomonas aeruginosa, odpowiedzialna za wypływ wielu antybiotyków, barwników, soli żółciowych oraz detergentów. Pompa ta składa się z trzech połączonych białek (AcrA, AcrB, oraz TolC ), ulokowanych w różnych częściach bakteryjnej ściany komórkowej. Wyrzut leku z wnętrza na zewnątrz komórki związany jest z transportem kationów wodorowych H+[3, 5].
Przeciw pompom białkowym. Strategia: zahamowanie aktywności transporterów białkowych stojących na straży bezpieczeństwa patogennych komórek. To „uśpienie czujności straży" ma uniemożliwić wychwyt antybiotyku bądź chemioterapeutyku przez pompę, dzięki czemu może on bezpiecznie dotrzeć do miejsca działania.
Jak uśpić czujność straży?
Jedną z najnowszych strategii w walce z lekoopornością jest poszukiwanie połączeń chemicznych hamujących aktywność transporterów białkowych stojących na straży bezpieczeństwa patogennych komórek. To swoiste „uśpienie czujności straży" może odbywać się na drodze różnych mechanizmów, które uniemożliwiają wychwyt antybiotyku bądź chemioterapeutyku przez pompę, dzięki czemu może on bezpiecznie dotrzeć do miejsca działania. W założeniu substancja o działaniu hamującym aktywność pompy, tzw.
EPI (ang. Efflux Pump Inhibitor), byłaby podawana równocześnie z antybiotykiem bądź cytostatykiem (lekiem hamującym rozwój nowotoworów), blokując tym samym jego wyrzut z komórki i zwiększając skuteczność terapeutyczną. Prace nad tym zagadnieniem są stosunkowo nowe i dotychczas udało się zidentyfikować tylko nieliczne rodziny związków chemicznych o działaniu EPI, z których żaden nie doczekał się jeszcze zastosowania terapeutycznego.
Poszukiwanie nowych substancji o działaniu EPI jest dużym wyzwaniem i nadzieją na poprawę skuteczności terapii wielu chorób. Pierwsze substancje wykazujące zdolność hamowania białkowych pomp wyrzutu zidentyfikowano wśród znanych leków i substancji biologicznie czynnych. I tak na przykład jednym z najbardziej popularnych inhibitorów pompy nowotworowej glikoproteiny P (P-gp) jest werapamil – znany lek przeciwarytmiczny. W przypadku trójdzielnych pomp lekooporności bakterii Gram-ujemnych, właściwości hamujące wykazują związki o budowie przypominającej fragmenty białek, tzw. peptydomimetyki.
Biorąc pod uwagę wysoki popyt na znalezienie substancji o charakterze EPI, które mogą udoskonalić terapię chorób o podłożu mikrobiologicznym czy nowotworowym, poszukiwania takie są przedmiotem intensywnych badań prowadzonych w Katedrze Technologii i Biotechnologii Środków Leczniczych UJ CM. W pracach wykorzystywane jest wspomagane komputerowo projektowanie, chemiczna synteza organiczna oraz testy biologiczne.
Zrealizowane do tej pory dwa projekty badawcze pozwoliły na zidentyfikowanie substancji aktywnych w grupie pochodnych hydantoiny (imidazolidyno-2,4-dionu), uzyskanych na bazie fenytoiny, czyli znanego leku przeciwpadaczkowego i przeciwarytmicznego. W tej grupie znaleziono związki hamujące P-gp znacznie mocniej niż werapamil. Dalsze poszukiwania będą przedmiotem nowych badań. Prace prowadzone przez zespół naukowców z UJ pozwoliły też uzyskać nowe związki o działaniu EPI wobec trójdzielnej pompy lekooporności bakterii Gram-ujemnych, które dają nowe perspektywy na poprawę terapii chorób wywołanych przez tzw. „alarmowe patogeny".
Projektor Jagielloński 2, "Zatrzymać lekooporne patogeny", www.projektor.uj.edu.pl
Tagi: terapia, lek, farmakoterapia, lekoopornosc
wstecz Podziel się ze znajomymi



Najdokładniejsze systemy satelitarnego transferu czasu
Nie zawsze zegar atomowy działa lepiej niż kwarcowy.

Ponad połowa chorych z SARS-CoV2 cierpi na długi covid
Przez długi czas może mieć takie objawy jak zmęczenie.



Uniwersytet Warszawski będzie kształcić kadry dla energetyki jądrowej
Przekazał Wydział Fizyki UW.










Recenzje