- Biochemia
- Biofizyka
- Biologia
- Biologia molekularna
- Biotechnologia
- Chemia
- Chemia analityczna
- Chemia nieorganiczna
- Chemia fizyczna
- Chemia organiczna
- Diagnostyka medyczna
- Ekologia
- Farmakologia
- Fizyka
- Inżynieria środowiskowa
- Medycyna
- Mikrobiologia
- Technologia chemiczna
- Zarządzanie projektami
- Badania kliniczne i przedkliniczne
Znaczenie Atomowej Spektroskopii Absorpcyjnej w mineralogii i geochemii
Wykorzystuje się tutaj absorpcję promieniowania elektromagnetycznego przez atomy, co powoduje przejście elektronu walencyjnego z poziomu podstawowego na poziom wzbudzony. Emisja promieniowania jest związana z przejściem elektronu z poziomu wzbudzonego na poziom podstawowy. Efektem absorpcji i emisji jest powstanie linii widmowych. Pomiar tych linii daje nam możliwość oznaczenia ilości danego pierwiastka w próbce (Fig. 1).
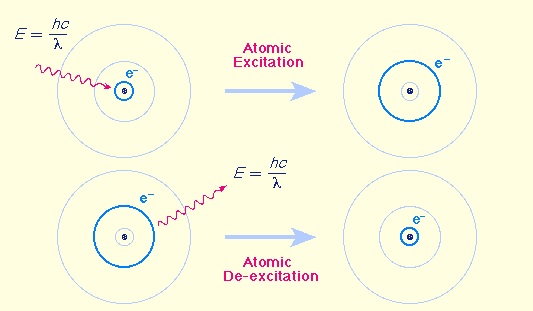
Miarą zawartości oznaczanego pierwiastka jest wielkość zaabsorbowanego przez niego promieniowania.
Budowa Atomowego Spektrometru Absorpcyjnego:
• Źródło promieniowania charakterystycznego (lampa)
• Atomizer (umożliwia wytworzenie gazu atomowego, powoduje oddzielenie od innych pierwiastków i przejście pierwiastków na poziom atomowy)
• Monochromator (np. siatka dyfrakcyjna; wydzielana jest tylko jedna linia rezonansowa dla żądanego pierwiastka)
• Detektor (fotopowielacz)
• Wzmacniacz
• Wskaźnik, komputer
W spektroskopii atomowej stosuje się specjalne lampy zawierające atomy, które są pobudzane do emisji promieniowania oznaczanego pierwiastka. Każdy pierwiastek musi być analizowany osobno przy użyciu innego rodzaju lampy. Wymiennie stosuje się:
• Lampa z katodą wnękową (HCL) – lampa z wyładowaniem elektrodowym, zawiera katodę i anodę; katoda zbudowana jest z pierwiastka analizowanego;
• Lampa z wyładowaniem bezelektrodowym (EDL) – brak katody, materiał sproszkowany zbudowany z oznaczanego pierwiastka; stosuje się do oznaczania pierwiastków, które trudno wzbudzić (o wysokim potencjale wzbudzenia).
Wywołanie efektu absorpcji atomowej wymaga atomizacji próbki, czyli jej odparowania i dysocjacji cząsteczek na atomy. Próbka przechodzi do roztworu a później do gazu atomowego. Przejście od roztworu do gazu atomowego składa się z dwóch etapów:
1) Nebulizacji – rozproszenie analizowanego roztworu w mgłę i przeprowadzenie jej w sposób jednorodny do płomienia
2) Atomizacji – zachodzi w płomieniach palnika, do którego doprowadza się gaz utleniający (powietrze, tlen lub podtlenek azotu), gaz palny (acetylen, propan butan) i roztwór analizowanej substancji w postaci aerozolu.
Zadaniem monochromatora jest eliminacja promieniowania własnego płomienia i wycięcie linii rezonansowej z promieniowania emitowanego przez lampę z katodą wnękową (źródła promieniowania liniowego). Spektrometry działają w zakresie fal od 193,7 do 852,1 nm.
Detektor (fotopowielacz) jest odpowiedzialny za pomiar natężenia promieniowania. Wytworzony w fotopowielaczu sygnał zostaje wzmocniony i w postaci analogowej wysyłany jest do komputera [1][2][3].
Metoda AAS jest typową metodą porównawczą, dlatego metodyka oznaczeń jest oparta na trzech znanych sposobach kalibracji: metodzie krzywej wzorcowej; metodzie dodawania wzorca; metodzie wzorca wewnętrznego [3].
Metodą Atomowej Spektroskopii Absorpcyjnej można oznaczyć około 70 pierwiastków. Służy ona przede wszystkim do wyznaczania pierwiastków śladowych i składników pobocznych. Jest to technika stosowana w laboratoriach geologicznych, metalurgicznych, medycznych, rolniczych oraz ochrony środowiska [3].
Na podstawie wprowadzenia analitu i rodzaju atomizera można wyróżnić: FAAS (flame atomic absorption spectrometry) – atomowa spektrometria absorpcyjna z atomizacją w płomieniu, ETAAS (electrothermal atomic absorption spectrometry) – atomowa spektrometria absorpcyjna z atomizacją elektrotermiczną, CVAAS (cold vapour absorption spectrometry) – technika zimnych par w atomowej spektrometrii absorpcyjnej [7].
Atomowa spektrometria absorpcyjna z atomizacją w płomieniu posłużyła między innymi badaniom oznaczenia obecności kadmu, miedzi oraz ołowiu w wodzie morskiej oraz wodzie mineralnej. Ze względu na niskie zawartości jonów metali w wodzie morskiej i mineralnej trudnym zadaniem jest bezpośrednie oznaczenie tychże metali. Stymulacja zawartością jonów chloru Cl- oraz siarczanowych SO32- w roztworach podczas badań wskazała, iż ilość tychże jonów nie ma wpływu na końcowe wyniki oznaczeń metali. Czynnikami istotnymi były odczyn pH roztworu (regulowany zawartością Na2CO3), oraz czas wirowania roztworu. Najlepsze wyniki otrzymano przy odczynie równym 7 oraz czasie wirowania równym co najmniej 20 minut [4]....
Autor: Julia Zdera
Artykuł do pobrania w załączniku.
Pobierz:
Zanczenie ASA w mineralogii i geologii
Tagi: atomowa spektroskopia absorpcyjna, lab, laboratorium, biotechnologia, ochrona środowiska, metale ciężkie, pierwiastki śladowe, minerał
wstecz Podziel się ze znajomymi









Recenzje