- Biochemia
- Biofizyka
- Biologia
- Biologia molekularna
- Biotechnologia
- Chemia
- Chemia analityczna
- Chemia nieorganiczna
- Chemia fizyczna
- Chemia organiczna
- Diagnostyka medyczna
- Ekologia
- Farmakologia
- Fizyka
- Inżynieria środowiskowa
- Medycyna
- Mikrobiologia
- Technologia chemiczna
- Zarządzanie projektami
- Badania kliniczne i przedkliniczne
Zdarzenia niepożądane towarzyszące badaniom klinicznym i możliwości ich zapobiegania cz.I
 Co roku w Polsce przeprowadzanych jest kilkaset badań klinicznych. Każde badanie kliniczne niesie ze sobą ryzyko wystąpienia tzw. działań niepożądanych, a także wiele korzyści materialnych i niematerialnych. Zazwyczaj działania niepożądane kojarzone są z pacjentami, czyli osobami, na których dane badanie jest przeprowadzane, jednakże w rzeczywistości na zagrożenia te narażone są także pozostałe osoby zaangażowane w badanie.
Co roku w Polsce przeprowadzanych jest kilkaset badań klinicznych. Każde badanie kliniczne niesie ze sobą ryzyko wystąpienia tzw. działań niepożądanych, a także wiele korzyści materialnych i niematerialnych. Zazwyczaj działania niepożądane kojarzone są z pacjentami, czyli osobami, na których dane badanie jest przeprowadzane, jednakże w rzeczywistości na zagrożenia te narażone są także pozostałe osoby zaangażowane w badanie.- włączeniu do badania klinicznego osoby, która nie wyraziła świadomej zgody na udział (powodem może być błędna interpretacja intencji potencjalnego uczestnika badania),
- braku przestrzegania prawa uczestnika do wycofania z badania w każdym momencie jego trwania,
- braku przestrzegania zasad ochrony prywatności (tj. brak przestrzegania zasad ochrony danych osobowych , a także zasad anonimizacji uczestnictwa wdanym badaniu) [3].
- wystąpienia działań i zdarzeń niepożądanych ( w tym zdarzeń ocenianych jako ciężkie),
- niewłaściwej opieki lekarskiej w trakcie trwania badania klinicznego,
- braku stosowania procedur medycznych, przewidzianych w danym badaniu klinicznym [3].
Należy mieć na uwadze, że zagrożenie bezpieczeństwa uczestnika może wynikać także z niewłaściwego oszacowania stosunku ryzyka do spodziewanych korzyści leczniczych, związanych z prowadzeniem danego badania. W niektórych przypadkach, do powstania szkody może przyczynić się niefrasobliwa postawa uczestnika, który to np. lekceważy przekazane mu zalecenia medyczne (wynikająca z niedostatecznej informacji o zagrożeniach i obowiązkach uczestnika badania klinicznego) [3].
Badania kliniczne i ich wpływ na gospodarkę
Każde badanie kliniczne ma oczywisty wpływ na gospodarkę. Prowadzenie badań klinicznych jest niezbędne do ogólnego rozwoju medycyny: dzięki nim możliwe staje się wprowadzenie na rynek skuteczniejszych, bezpieczniejszych, a tym samym bardziej zaawansowanych leków. Co ważne, badania kliniczne wywierają bezpośredni wpływ na gospodarkę oraz na społeczeństwo kraju, w który są prowadzone.
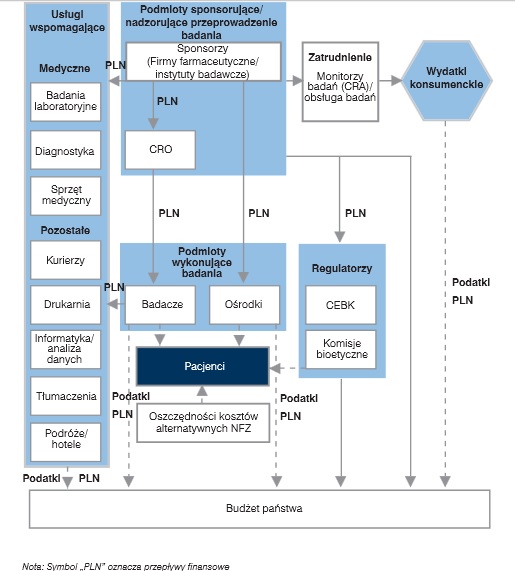
Wśród najczęściej dostrzeganych pozytywów przeprowadzania badań klinicznych należy wymienić:
- wpływ na różne sektory gospodarki (sektor opieki medycznej, inne sektory powiązane z rynkiem badań)
- prowadzenie badań klinicznych przez duże międzynarodowe firmy farmaceutyczne przyczynia się do zwiększonego napływu środków pieniężnych do naszej gospodarki [4].
- badaczy(lekarze prowadzący dany eksperyment)
- sponsorów badania klinicznego
- firmy farmaceutyczne (mające za zadanie finansowanie i częściową realizację badania klinicznego)
- ośrodki (tj. szpitale, poradnie, gabinety lekarskie, w których badanie kliniczne się odbywa)
- monitorów badań klinicznych (tj. firmy prowadzące i zarządzające badaniami) [1], [2].
By skutecznie zapobiegać zagrożeniom, które mogą występować w trakcie prowadzenia badania klinicznego, wymagane jest opracowanie skutecznych metod ujawniania i analizy zagrożeń. Ograniczanie ryzyka osiąga się poprzez:
- szkolenia,
- trening,
- nadzór oraz system kar i środków dyscyplinujących.
W trakcie realizacji badań mogą wystąpić następujące szkody:
- fizyczne, które polegają na poniesieniu trwałego lub przemijającego uszczerbku na zdrowiu
- szkody dotyczące psychiki (w większości polegające na niekorzystnym postrzeganiu swojej osoby,ujawnianiu sie emocji takich jak strach czy poczucie winy)
- szkody w sferze stosunków społecznych (pojawienie się niekorzystnych relacji międzyludzkich, takich jak: dyskryminacja, stygmatyzacja, ostracyzm, utrata dobrego imienia)
- szkody prawne (oskarżenie, aresztowanie, proces sądowy) lub szkody materialne (straty ekonomiczne)
- szkody dotyczące godności osobistej lub szkody wynikające z zerwania relacji lub zobowiązań pomiędzy podmiotami, które zaangażowane są w realizację danego badania klinicznego, naruszanie prywatności, zwyczajów i zachowań
Analiza zagrożenia w badaniach klinicznych
Rozpoczęcie analizy potencjalnego zagrożenia
Literatura:
[2]. Czarkowski M., 2008 .Zagrożenie, ryzyko i szkoda w badaniach klinicznych. Artykuł redakcyjny.
[3]. http://www.sarcoma.pl/badania-kliniczne/zagrozenie-stopien-ryzyka-i-szkoda-w-badaniu-klinicznym/
[4].http://infarma.pl/fileadmin/badania_kliniczne_raport/Badania%20kliniczne%20w%20Polsce%202010.pdf’
[5].MRC/DH joint project to codify good practice in publicly-funded UK clinical trials with medicines. Workstream 4: Trial Management and Monitoring, 2004, http://www.ct-toolkit.ac.uk/_db/_documents/Trial_RA.pdf
[6]. http://unesdoc.unesco.org/images/0014/001461/146180E.pdf
[7]. USTAWY z dnia 6 września 2001 r. Prawo farmaceutyczne (Rozdział 1 Przepisy ogólne, Art.2)
[8]. Rozporządzenie Ministra Zdrowia z 07 kwietnia 2005 w sprawie trybu i zakresu prowadzenia kontroli badań klinicznych. Dziennik Ustaw 2005, Nr 69, poz. 623.
Tagi: zagrożenia badania klinicznego, działania niepożądane, naruszenie praw uczestnika, wpływ badań klinicznych na gospodarkę, szkody w badaniach, analiza zagrożeń
wstecz Podziel się ze znajomymi









Recenzje