- Biochemia
- Biofizyka
- Biologia
- Biologia molekularna
- Biotechnologia
- Chemia
- Chemia analityczna
- Chemia nieorganiczna
- Chemia fizyczna
- Chemia organiczna
- Diagnostyka medyczna
- Ekologia
- Farmakologia
- Fizyka
- Inżynieria środowiskowa
- Medycyna
- Mikrobiologia
- Technologia chemiczna
- Zarządzanie projektami
- Badania kliniczne i przedkliniczne
Barwniki naturalne - teoria i praktyczne zastosowanie
Tabela 1. Zestawienie par barw zasadniczych i dopełniających.
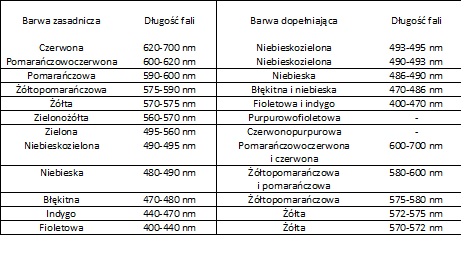
Efekt koloru dowolnego ciała lub ośrodka nie świecącego polega na wywoływaniu wrażenia barwy pod wpływem promieniowania oświetlającego. Zabarwienie ciał jest wynikiem różnorodnych procesów fizycznych. Najważniejszym jest selektywne pochłanianie. W najprostszym przypadku zjawisko to obserwuje się przy przechodzeniu światła przez ośrodek pochłaniający promieniowanie o pewnych długościach fali, odpowiadających określonym obszarom widma. Barwa takiego ciała jest wrażeniem będącym efektem złożenia tych wszystkich części widma widzialnego, które nie uległy pochłonięciu przez ośrodek. Taki typ zabarwienia wykazuje kolorowe szkło. Pochłanianie selektywne jest również przyczyną zabarwienia ciał rozpraszających. W tym przypadku światło padające na obiekt wnika w niego na pewną głębokość, ulegając pochłanianiu w pewnym obszarze widma, i następnie wychodzi z powrotem jako światło rozproszone o zmienionym składzie widmowym. Efekt taki obserwuje się w przypadku liści czy też powierzchni pokrytych farbą.
Innym procesem fizycznym jest selektywne odbicie. Efekt ten występuje wtedy gdy selektywne pochłanianie staje się bardzo silnie. Zdolność odbijająca jest wówczas największa dla promieniowania o tej długości fali, która ulega najsilniejszemu pochłanianiu. Należy zwrócić uwagę, iż w tym przypadku barwa w świetle przechodzącym jest inna niż w odbitym i mają się one do siebie na ogół jak barwy dopełniające. Zabarwienie na skutek selektywnego odbicia wykazują przede wszystkim metale.
Należy również powiedzieć o rozproszeniu światła na skutek niejednorodności ośrodka. W przypadku gdy rozmiary niejednorodności są porównywalne z długością fali, obserwuje się zabarwienie wynikające z różnic w rozpraszaniu promieniowania. Najsilniej rozpraszane są fale najkrótsze (tj. niebieskie i fioletowe), natomiast najsłabiej najdłuższe (czerwone). Rozpraszanie jest efektem błękitnego zabarwienia nieba.Zabarwienie na skutek interferencji obserwowane jest głównie przy odbiciu wiązki światła od dwóch powierzchni ograniczających cienką, przezroczystą warstwę przy czym dla danego kąta padania i danej grubości warstwy w świetle odbitym wygaszone zostają te barwy, dla których różnice dróg optycznych wynoszą nieparzystą wielokrotność połowy długości fali.
Pomiary fotokolorymetryczne
Absorpcja światła widzialnego przez różne materiały jest uwarunkowana pochłanianiem kwantów promieniowania przez dane cząsteczki. Energia fotonów światła widzialnego (Vis) i ultrafioletowego (UV) zużywana jest do wzbudzenia stanów elektronowych molekuł. Energia potrzebna na wzbudzenie elektronów należących do różnych typów atomów lub wiązań w cząsteczce jest różna, zatem przez różne związki absorbowane są różne długości fali. Najwyższa energia potrzebna jest do wzbudzenia elektronów walencyjnych tworzących wiązanie pojedyncze i odpowiada promieniowaniu z zakresu dalekiego ultrafioletu, mniejsza zaś na wzbudzenie elektronów wiązań podwójnych oraz elektronów orbitali d-elektronowychjonów metali. Atomy i grupy funkcyjne odpowiedzialne za absorpcje światła, a tym samym nadawanie materii barwy nazywamy chromoforami. Są to najczęściej wiązania podwójne pomiędzy atomami węgla, węgla i azotu, tlenu i siarki, grupy nitrowe oraz całe układy aromatyczne. Silną absorpcję światła widzialnego wykazują także niektóre jony metali d- i f-elektronowe. Jeśli dwa lub więcej układów chromoforowych występuje w bezpośrednim sąsiedztwie, dochodzi pomiędzy nimi do sprzężenia, czego efektem jest przesunięcie pasma absorpcji w stronę fal dłuższych.
Wiele grup funkcyjnych przyłączonych do chromoforu lub sprzężonego układu chromoforów powoduje zmianę długości fali absorbowanej przez związek oraz intensywności tej absorpcji. Podstawniki takie nazywamy auksochromami (halogeny, grupy hydroksylowe i aminowe). Efekt ten polega na oddziaływaniu podstawnika z elektronami chromoforu, skutkiem czego są zmiany energii potrzebnych na ich wzbudzenie. Zmiany podobne jak na skutek działania auksochromów obserwuje się często pod wpływem rozpuszczalnika.
W przypadku gdy zmiana położenia pasma absorpcji następuje w stronę większych długości fali (mniejszych częstości) mówimy o przesunięciu batochromowym (przesunięcie ku czerwieni), jeśli w stronę przeciwną, to mówimy o przesunięciu hipsochromowym (przesunięcie w stronę fioletu). Zwiększenie intensywności pasma absorpcji pod wpływem podstawnika lub rozpuszczalnika nazywamy efektem hiperchromowym, zaś zmniejszenie nazywamy efektem hipochromowym.
Podstawą fotokolorymetrii jest prawo Berra, obowiązujące dla roztworów gazowych, ciekłych i stałych o niezbyt dużym stężeniu. Stwierdza ono, że natężenie światła monochromatycznego (I), przechodzącego przez warstwę pochłaniającą o grubości (l)i o stężeniu substancji pochłaniającej promieniowania wynoszącym (c), maleje wykładniczo. Logarytm naturalny ze stosunku natężeń wiązki padającej do przechodzącej przez ośrodek nazywamy absorbancją (A).
Flawonoidy
Związki flawonoidowe są głównymi barwnikami kwiatów i owoców (czasami również innych części rośliny) [1,2]. Mają zabarwienie od kremowożółtego do niebieskiego, niektóre zaś są bezbarwne i pełnią inne funkcje fizjologiczne. Dzielone są na kilka zasadniczych klas, w zależności od charakteru mostka trówęglowego. Zmienność w obrębie każdej z klas wynika z ilości i lokalizacji w cząsteczce grup hydroksylowych, możliwości tworzenia przez nie połączeń eterowych (najczęściej z alkoholem metylowym), estrowych oraz miejsca przyłączenia i charakteru grup glikozydowych (Rys. 1).
Flawonoidy mogą być zarówno mono- jak i poliglikozydami, zawierającymi reszty jedno- jak i oligosacharydowe (największe bogactwo pochodnych cukrowych wykazuje kwercetyna, ponad osiemdziesiąt związków).
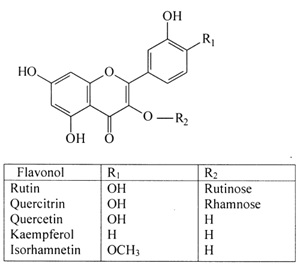
Rysunek 1. Struktura flawonoidu z przykładami związków różniących się podstawnikami R1 i R2 [3].
Obecnie obowiązujący podział flawonoidów obejmuje flawanony, flawony, flawonole, izoflawony, antocyjaniany, katechiny i biflawony (biflawonoidy).
Karotenoidy
Karotenowce występują zarówno u roślin wyższych, glonów, sinic i bakterii jak również w tkankach niektórych, niezdolnych do fotosyntezy, grzybów [4,5]. W komórkach roślinnych zlokalizowane są głównie z chloro- jak i chromoplastach. W procesie fotosyntezy odpowiedzialne są za pochłanianie energii świetlnej niesionej przez kwanty promieniowania widzialnego odpowiadające długościom fal nie absorbowanych przez chlorofile. Pełnią ponadto funkcje ochronne, selektywnie pochłaniając niepożądane częstotliwości fal świetlnych. Są prekursorami hormonów roślinnych i naturalnych substancji zapachowych. Są one związkami macierzystymi z których powstaje witamina A. Wchodzą również w skład błon komórkowych gdzie pełnią funkcje antyoksydantów. Mają barwy od czerwonej do żółtej czasami o odcieniu brązowozielonym. Barwniki z tej grupy nadają kolor wielu owocom (cytrusy, truskawki, papryka, pomidory), liściom (ich kolor jest zazwyczaj maskowany przez chlorofile, uwidacznia się jednak często, np. jesienią, kiedy to barwnik zielony ulega rozkładowi), kwiatom (narcyzy) oraz niektórym zwierzętom (pióra kanarka, wiele owadów, tkanki łososia).Głównymi przedstawicielami karotenów są β-, α- i γ-karoten, przy czym izomer β- stanowi 75-80% ogółu karotenów roślinnych i jest zarazem głównym prekursorem witaminy A (Rys. 2).
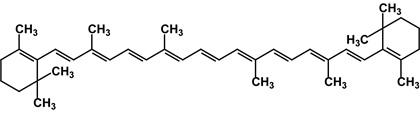
Rysunek 2. Struktura β-karotenu [6].
Cząsteczki wyżej wymienionych związków zawierają fragmenty cykliczne. Znane są także karoteny otwartołańcuchowe. Przykładem może być neurosporen izolowany z grzybów i likopen występujący w pomidorach i papryce. Cząsteczki zawierające tylko jeden pierścień bądź nie zawierające go wcale są na ogół produktami pośrednimi na drodze syntezy związków o dwóch pierścieniach w molekule. Ksantofile sąpochodnymi karotenów zawierają, zazwyczaj umieszczone symetrycznie, grupyalkoholowe, karboksylowe, aldehydowe, ketonowe i epoksydowe. Występują, obok karotenowców, w tkankach roślinnych i zwierzęcych. Najczęściej spotykane są pochodne o charakterze alkoholi i epoksydów. Najprostszym związkiem z tej klasy jest luteina (ksantofil), będąca 3,3’-dihydroksypochodną α-karotenu. Występuje praktycznie w tkankach wszystkich roślin zielonych. Rzadziej spotykane w świecie roślinnym są pochodne ketonowe (np. rodoksantyna z igieł cisa pospolitego), jednakże stanowią one jedne z ważniejszych ksantofili zwierzęcych. Z form niesymetrycznie podstawionych wymienić należy kryptoksantynę (pomarańczowy barwnik owoców papryki i pomarańczy) oraz fukoksantynę, która jest barwnikiem brunatnic uczestniczący w fotosyntezie.Na drodze degradacji karotenoidów powstaje kilka ważnych barwników naturalnych. Najważniejszym jest witamina A (retinal), będąca niebiałkowym składnikiem rodopsyny, która odpowiedzialna jest za odbieranie bodźców świetlnych przez liczne zwierzęta i niektóre organizmy roślinne (bakterie i glony jednokomórkowe). Mechanizm widzenia opiera się na procesie izomeryzacji jednego z wiązań podwójnych w cząsteczce retinalu.
Barwniki porfirynowe
Chlorofile są zielonymi barwnikami porfirynowymi zawierającymi skoordynowany atom magnezu (Rys. 3). Mają fundamentalne znaczenie w procesie fotosyntezy. W chloroplastach występują w formie związanej z białkami. W chlorofilu do pierścienia porfirynowego przyłączone są liczne podstawniki, determinujące właściwości fotochemiczne cząsteczki. Cząsteczki chlorofili zawierają dwie grupy karboksylowe, z których jedna jest zawsze zestryfikowana długołańcuchowym niepolarnym alkoholem (najczęściej tzw. fitolem). Zawartość chlorofili w zielonych tkankach roślin wynosi około 10% ich suchej masy.
Rysunek 3. Struktury hemu oraz chlorofili A i B [8]
Barwniki hemowesą kompleksami protoporfiryny IX z jonami żelaza(II) (tzw. ferrohem) lub żelaza(III) (tzw. ferrihem). Barwniki te wchodzą w skład licznych chemoprotein, odpowiedzialnych za transport tlenu (hemoglobina), jego magazynowanie w tkankach (mioglobina), transport elektronów (cytochromy) oraz pełniących funkcje enzymatyczne (katalazy, peroksydazy). Mają one zabarwienie czerwone lub brunatnoczerwone. Fragment porfirynowy jest związany z białkiem bądź poprzez wiązania koordynacyjne, bądź kowalencyjne (poprzez podstawniki winylowe).
Barwniki pirolowewystępują w organizmach roślinnych (fikobiliny) i zwierzęcych (bilany). Związki z tej grupy zawierają, podobnie jak porfiryny, cztery pierścienie pirolowe, z tym że w tym wypadku nie tworzą one struktury cyklicznej. Mają zabarwienie od żółtobrunatnego poprzez pomarańczowe do czerwonofioletowego i niebieskiego. Fikobiliny pełnią funkcje barwników asymilacyjnych, absorbując światło w zakresie długości fali nie pochłanianych przez chlorofile (tzw. barwniki wspomagające). W zależności od barwy kompleksu białkowo-fikobilinowego rozróżnia się fikocyjaniny (niebieskofioletowe) i fikoerytryny (czerwone). Fikobiliny roślin wyższych to tzw. fitochromy. Są one, podobnie jak u roślin niższych, połączone z fragmentem białkowym. Kompleksy te uczestniczę w wielu procesach fizjologicznych regulowanych przez światło, regulują ekspresję genów, syntezę i aktywność enzymów oraz szybkość metabolizmu. Chromofor fitochromów występuje w dwóch formach, różniących ię widmem absorpcyjnym i ulegających wzajemnym przemianom pod wpływem światła oraz specyficznych układów enzymatycznych.
Barwniki chinonowe
Różnorodna pod względem struktury, biosyntezy i funkcji grupa pigmentów zawierających w cząsteczkach fragment benzo-, nafto-, antro- lub fenantrochinonu, nazywana jest chinonami. Większość z nich występuje w formie glikozydów. Charakteryzują się żółtym, pomarańczowym bądź czerwonym zabarwieniem. Wiele ze związków chinonowych występuje w świecie roślinnym (a także zwierzęcym), pełniąc różnorakie funkcje fizjologiczne nie związane bezpośrednio z ich zabarwieniem. Obok nich izoluje się z roślin wiele innych substancji o nie do końca wyjaśnionej roli biologicznej. Niektóre z nich są barwnikami kwiatów, drewna, liści, korzeni, antybiotykami (adriamycyna) (Rys. 4).
Rysunek 4. Struktura adriamycyny [9].
Inne odgrywają dużą rolę w alopatii lub jako toksyny produkowane przez rośliny wyższe i będące substancjami obronnymi przed szkodnikami oraz patogennymi mikroorganizmami, kolejne powstają w mikroorganizmach i służą jako toksyny skierowane przeciwko roślinom i zwierzętom. Wiele substancji chinonowych jest odpowiedzialnych za barwę grzybów wyższych.
Barwniki diterpenowe
Obok karotenoidów, stanowiących najliczniejszą grupę barwników o charakterze terpenowym znanych jest kilka innych barwników izoprenoidowych, zawierających trzy lub cztery pierścienie zbudowane z dwudziestu atomów węgla. Pigmenty te odznaczają się barwą pomarańczową do ciemnoczerwonej. Większość z nich zawiera w swoich molekułach ugrupowanie chinonowe, jednakże ze względu na drogę biosyntezy zaklasyfikowano je jako odrębną grupę. Substancje te dzieli się na trzy klasy, a mianowicie tanschinony, rojleanony oraz koleony.
Barwniki alkaloidowe
Alkaloidy stanowią ważną grupę metabolitów roślinnych o różnorodnej budowie i funkcjach fizjologicznych. Niektóre z nich pełnią rolę barwników. Najważniejszymi przykładami są berberyna oraz betaksantyny i betacyjaniny (Rys. 5). Betaksantyny stanowią grupę żółtych barwników. Są pochodnymi aminokwasów alifatycznych, wykazującymi charakter zasad Schiffa.
Rysunek 5. Struktura berberyny.
Do najważniejszych przedstawicieli należy indykaksantyna i wulgaksantyna (barwniki bulwy buraka pastewneg).
Inne barwniki zwierzęce
Obok opisanych powyżej barwników wchodzących w skład tkanek zwierzęcych wymienić należy jeszcze kilka, należących do mniej licznych, ale zarazem bardzo istotnych grup.
Melaniny należą do heteropolimerów o złożonej i zróżnicowanej budowie. Nadają one kolor włosom, skórze oraz tęczówce. Wywodzą się z tyrozyny. Często zawierają dodatkowe podstawniki, pochodzące z układów terpenoidowych lub pirolowych. W zależności od składu dzielimy je na feomelanini - wielkocząsteczkowe produkty polimeryzacji benzotiazyn, kolor czarny i ciemnobrązowy, trichochromy - związki podobne do feomelanin, lecz charakteryzujące się mniejszą masą cząsteczkową, eumelaniny - produkty kondensacji dopachinonu i dopachromu, kolor żółty do jasnobrązowego oraz melaniny typu mieszanego.
Podsumowanie
Barwniki naturalne pełnią wiele funkcji ważnych dla życia zarówno roślin, jak i zwierząt. Chlorofile i karotenoidy biorą udział w procesie fotosyntezy. Inne barwniki uczestniczą w procesach oksydoredukcyjnych, nadają kolor kwiatom, owocom, liściom. Związki barwne ze względu na swoje właściwości, takie jak barwa czy aktywność biologiczna, znajdują także szerokie zastosowanie w przemyśle spożywczym, odzieżowym, w lecznictwie i w przemyśle farmaceutycznym.W komórkach roślinnych barwniki występują rzadko w postaci wolnej, często są związane z cukrami jako glikozydy, rzadziej z białkami. Barwniki, które rozpuszczają się w wodzie (antocyjany, betalainy) znajdują się w soku komórkowym, natomiast te, które rozpuszczają się w tłuszczach występują w plastydach - chlorofil w chloroplastach, a karotenoidy w chromoplastach.
O barwie związku decyduje jego struktura chemiczna. Barwniki stanowią niejednolitą grupę związków pod względem budowy chemicznej. Wyróżnia się wśród barwniki zielone - chlorofile, karotenoidy (karoteny, ksantofile) o zabarwieniu żółtym, pomarańczowym, czerwonym, oraz fioletowym.
Związki zawierające azot to ryboflawina o barwie żółtej, betalainy, a wśród nich betacyjaniny o barwie od czerwonej aż do fioletowej oraz żółto-pomarańczowe betaksantyny. Flawonoidy to barwniki żółte. Antocyjany w zależności od pH odznaczają się barwą czerwoną, fioletową lub niebieską. Chinony, wśród których wyróżnia się antrachinony, naftochinony i benzochinony, to związki o barwie żółtej, pomarańczowej, poprzez czerwoną aż do brunatnej. Innymi ważnymi barwnikami pochodzenia roślinnego są indygo oraz kurkumina.
Przedstawiona paleta barw tworzona przez barwniki naturalne stwarza ogromne możliwości w barwieniu produktów spożywczych, jak i przemysłowych przyjaznych dla zdrowia i środowiska.
Autor: Karolina Wójciuk
Literatura:
1. Kandaswami, C., Middleton, E. Jr., 1994.Free radical scavenging and antioxidant activity of plant flavonoids.Adv. Exp. Med. Biol., 366:351-76
2. Samman, S., Soto, C., Cooke, L., Ahmad, Z., Farmakalidis, E., 1996. Is erythrocyte alkaline phosphatase activity a marker of zinc status in humans?. Biol. Trace Elem. Res., 51(3), 285-91
3. http://rozanski.li/?p=52
4. Isler O., 1971. Carotenoides, Chemical Research Department, Zurich
5. Karrer P., Jucker E., 1948. Carotenoide, Birkhause Verlag
6. http://commons.wikimedia.org/wiki/File:Beta-carotene.png
7. Bojarski J., Chemia organiczna, Wydawnictwo Uniwersytetu Jagiellońskiego, Wydanie VI, Kraków 1999
8. http://chemfan.pg.gda.pl/Publikacje/Zobaczyc_zapach.html
9. http://pl.wikipedia.org/wiki/Doksorubicyna
10. http://www.czytelniamedyczna.pl/3873,glistnik-jaskolcze-ziele-chelidonium-majus-l-we-wspolczesnej-terapii-wskazania.html
Tagi: barwa podstawowa, barwa dopełniająca, widzenie, barwnik naturalny, barwnik syntetyczny, fotokolorymetria, flawonoidy, karotenoidy, porfiryny, chinony, diterpeny, alkaloidy
wstecz Podziel się ze znajomymi









Recenzje