Streszczenie
Większość znanych substancji jest diamagnetyczna bądź ferromagnetyczna. Tylko nieliczne oddziaływają z polem magnetycznym, są to paramagnetyki. Efekt tych oddziaływań jest także bardzo niski, ale możliwy dzięki nieparzystym elektronom w cząsteczkach lub niesparowanym elektronom w cząsteczkach rodników. Elektronowy Rezonans Paramagnetyczny (EPR) zwany także Elektronowym Rezonansem Spinowym (ESR) pozwala na rejestrację i badanie tego całkiem powszechnego, ale bardzo ważnego zjawiska w różnych dziedzinach nauki (chemia, biologia).
Wprowadzenie
Elektronowy rezonans paramagnetyczny (EPR) został odkryty i opisany w 1944 przez E. K. Zavoiskii. Zastosowanie tej metody w biologii rozpoczęło się dopiero w latach 60 XX wieku. I od tego czasu metoda badania próbek biologicznych metodą EPR jest ciągle szeroko dyskutowana w literaturze [ ]. Szeroki zakres badań próbek biologicznych zostało przeprowadzonych na mediach ustroju ludzkiego: krwii, moczu, ślinie itp. Badania te zostały przeprowadzone w celach diagnostyki medycznej.
Teoria
Elektronowy rezonans paramagnetyczny (EPR, ang. Electron Paramagnetic Resonance) jest związany ze zmianą orientacji spinu elektronowego w zewnętrznym polu magnetycznym, wywołanego absorpcją energii pola wysokiej częstości. Zjawisko to obserwuje sie w atomach, cząsteczkach i kompleksach molekularnych posiadających niesparowane spinowe momenty magnetyczne μs, tworzące centra paramagnetyczne badanych związków.
Moment magnetyczny μs i spin elektronu S centrum paramagnetycznego są kolinearne, ale przeciwnie skierowane:
μs = -g μBS
μs – magneton Bohra (9,27x10-24 JxT-1)
g – współczynnik zeemanowskiego rozszczepienia
Współczynnik rozszczepienia g określa udział orbitalnego momentu magnetycznego w całkowitym momencie μ danego centrum paramagnetycznego.
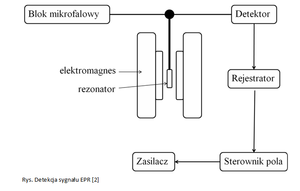
Dla spinu S=1/2 wartości magnetycznej liczby spinowej wynoszą: ms=+1/2 i ms=-1/2. Ze względu na dwie przeciwne orientacje spinu w polu magnetycznym możliwe są dwa poziomy energetyczne: W+1/2=½gμBB i W-1/2=-½gμBB, różnica energii (∆W= W+1/2-W-1/2) tych poziomów rośnie wraz z przyłożonym polem magnetycznym B. Zmiana orientacji spinu nastąpi, gdy zostanie spełniony warunek rezonansu ∆W = hf, czyli zostanie dostarczona energia równa różnicy energetycznej dwóch poziomów. Amplituda sygnału obserwowanego w rejestratorze jest miarą absorpcji mocy mikrofal wywołanej zmianą orientacji spinu elektronów względem kierunku stałego pola magnetycznego [ ].
Rys. Detekcja sygnału EPR [2]
Standardowa analiza EPR
Metoda EPR w badaniach biologicznych pozwala badać wolne rodniki lub metale, które w wyniku biochemicznych przemian redoks posiadają niesparowany elektron np. hemoglobina, która była jednym z pierwszych metaloenzymów zbadanych tą metodą. Badanie wolnych rodników w komórkach nie patogennych nie jest łatwe, gdyż naturalny poziom rodników jest bardzo niski (10-8-10-10M) a nowoczesne spektrometry EPR są wstanie zarejestrować wolne rodniki w stężeniu 10-6-10-7. Stężenie wolnych rodników można zwiększyć wykorzystując jednolity materiał tkankowy (1014-1016 na gram tkanki) lub traktując materiał biologiczny donorami wolnych rodników lub napromienienie. Intensywność sygnału EPR jest także zależna od fazy wzrostu komórek i fazy cyklu komórkowego. Dodatkową trudność w pomiarach biologicznych stwarza stosunkowo duża ilość wody, która uniemożliwia dokładne zarejestrowanie sygnału oraz pozwala na dalsze przemiany biochemiczne. Dlatego próbki te zazwyczaj badane są w temperaturze poniżej 0⁰C lub w postaci zliofilizowanej. [ , ]
Mimo wielu trudności w zastosowaniu metody EPR przy badaniu próbek biologicznych metoda ta pozwala jakościowo a nawet ilościowo oznaczyć rodniki w tych bardzo złożonych próbkach.
Pułapkowanie spinów
W roku 1965 w Rosji badaczom pierwszy raz udało się zarejestrować metodą EPR tlenek azotu(II) - NO. Rodnik ten posiada jeden niesparowany elektron przemieszczający się pomiędzy atomem azotu a atomem tlenu. NO został unieruchomiony i zablokowany wobec ewentualnych reagentów grupami metylowymi. W dalszy badaniach stwierdzono, że NO daje widma EPR, gdzie kształt ich zmienia się w zależności do lepkości, polarności i struktury otaczających go mediów. I tak powstała pierwsza sonda EPR, która po przyłączeniu do białek czy lipidów pozwala uzyskać informacje o miejscowej ruchliwości łańcucha polipeptydu. Badania nad sondami EPR pozwoliły określić struktury ciekłych kryształów i ruchliwości lipidów w membranach.
W biologii metoda „pułapkowania spinów” jest bardzo ważna w wykrywaniu reaktywnych form tlenu (RFT). Istota metody jest tworzenie paramagnetycznych adduktów w wyniku reakcji nitonów (związki azowe) z oznaczanymi rodnikami RFT. Powstały produkt jest bardziej stabilny niż oznaczany rodnik. Dodatkowo powstałe produkty różnią się miejscem akceptorowym elektronu w zależności od stabilizowanego rodnika co pozwala na jakościową analizę rodników. „Pułapki”, którymi są związki nitrowe różnią się od siebie nawzajem szybkością reakcji z rodnikami tlenowymi. Stałe szybkości tych reakcji są zazwyczaj małe dlatego tez wskazane jest stosowanie dużych stężeń pułapek spinowych (5-200 mmolxl-1). [ , ]
Niebawem dostępne będą banki danych zawierające parametry widm EPR adduktów pułapkowania, które pozwolą na dokładną identyfikację wolnego rodnika a będzie to możliwe w oparciu o widma EPR adduktów powstałych z pułapkowania.
Autor: Karolina Wójciuk
Tagi:
spektrometria,
elektronowy rezonans paramagnetyczny,
EPR,
elektronowy rezonans spinowy,
ESR,
paramagnetyzm,
lab,
laboratorium,
labortaoria
wstecz
Podziel się ze znajomymi









Recenzje