Platforma nanocząsteczek do stosowania w termoterapii raka
Hipertermia mikrofalowa jest jedną z najważniejszych klinicznych technik termoterapii ze względu na oczywiste korzyści nieinwazyjnego modelu ogrzewania, odpowiednią głębokość penetracji w tkankach oraz idealny potencjał zabijania komórek nowotworowych bez ryzyka chirurgicznego lub toksyczności chemioterapii.
Jednak często trudno jest zastosować ciepło lokalnie względem nowotworu. Typowo, kończyny lub inne części ciała, które zawierają nowotwór są ogrzewane zewnętrznie. Prowadzi to często do znacznego dyskomfortu pacjenta oraz uszkodzenia zdrowych tkanek otaczających guz.
Kontaktując ze sobą ekspertów w dziedzinie medycyny z ekspertami w dziedzinie nanotechnologii, naukowcy dążą do zbadania możliwości opracowania środków wrażliwych na mikrofale, które skupiają efekty destrukcyjne mikrofal konkretnie na komórkach nowotworowych.
Naukowcy z Technical Institute of Physics and Chemistry, Chinese Academy of Sciences ostatnio zaproponowali po raz pierwszy nowatorskie podejście do stosowanio mikro- oraz nanomateriałów jako środków podatnych na mikrofale w hipertermii nowotworowej in vivo.
"Nasze badanie pokazuje, że takie podejście hamuje wzrost guza i znacząco wydłuża przeżycia w modelu zwierzęcym," mówi Dr. Xianwei Meng, który nadzorował zespół badawczy.
"Nasze mikrokapsułki składają się z płynnego rdzenia z roztworów chlorku sodu (NaCl) oraz biokompatybilnego alginianiu sodu jako materiału ścian", tłumaczy Meng. "W obecności mikrofal absorbowana energia mikrofalowa jest zamieniana na energie kinetyczną oraz międzyjonową jonów i przechowywana jako energia grzewcza Joule'a jonów soli poprzez interakcje między jonami soli, co prowadzi do gwałtownego wzrostu temperatury."
Ze względu na właściwości doskonałej podatności na mikrofale oraz niską biotoksyczność, naukowcy osiągnęli idealną wydajność terapii ze współczynnikiem hamowania nowotworu na poziomie 97,85%.
Wraz z modelem symulacji komputerowej zespół potwierdził mechanizm wysokiej wydajności podgrzewania mikrofalami w teorii, wykazując, że wydajność odgraniczenia przestrzennego ścian mikrokapsułki nadaje jonom wewnętrznym duże właściwości podatności na mikrofale.
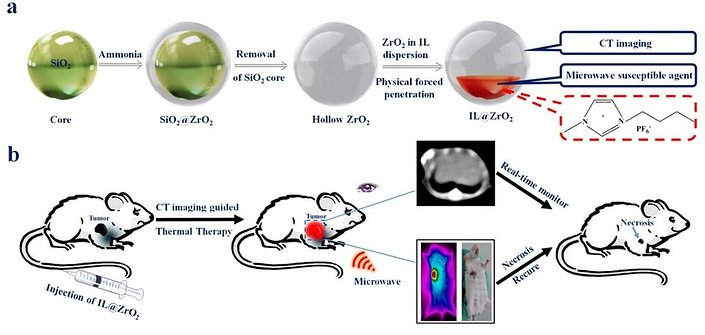
Wszystko to brzmi doskonale w teorii, a do badania dołączył Profesor Ke Xu z Oddziału Radiologii First Hospital of China Medical University. W dalszej kolejności zespół opracował prostą pustą nanostrukturę ZrO2 jako przenośnik zawierający jonowy płyn (IL@ZrO2).
Ta nowatorska nanocząsteczka łączy właściwości obrazowania za pomocą tomografii komputerowej z promieniami Rentgena (TK), pustych nanocząsteczek ZrO2 oraz wysoką wydajnością podgrzewania mikrofalami jonowego płynnego rdzenia.
"Kapsuła ZrO2 wytwarza wzmocniony efekt obrazowania TK który umożliwia wysoce czułą detekcję in vivo oraz in vitro, a jonowy płyn wewnątrz wytwarza efekt podatności na mikrofale który zapewnia doskonałą wydajność termoterapii," Meng podsumowuje wyniki.
(a) Schematyczna ilustracja syntezy pustych nanocząsteczek ZrO2 za pomocą metody matrycowej oraz opłaszczania IL za pomocą metody penetracji siłą fizyczną. (b) Schematyczna ilustracja IL@ZrO2 jako wielofunkcyjnego środka teranostycznego do kierowanej obrazowaniem TK mikrofalowej terapii termalnej in vivo oraz wizualnego monitorowania efektów terapeutycznych w czasie rzeczywistym. (Opublikowane przez The Royal Society of Chemistry)
Ta prosta nanostruktura może być użyta jako wielofunkcyjny środek teranostyczny poprzez połączenie modalności diagnostycznych oraz terapeutycznych w jednym "zestawie".
Według Menga, wyniki obrazowania in vitro oraz in vivo potwierdzają potencjał stosowania obrazowania TK do prowadzonego w czasie rzeczywistym monitorowania biodystrybucji i procesu metabolicznego, a także oceny wyników terapeutycznych. Wyniki terapeutyczne można ocenić wizualnie za pomocą obrazowania CT. W międzyczasie monitorowanie w czasie rzeczywistym dystrybucji ZrO2@IL in vivo może być osiągnięte za pomocą wzmocnionego obrazowania CT przez modele miniaturowych świń bez ofiar zwierząt z partii eksperymentalnych w różnych punktach po zastrzyku, co zgłaszano w poprzednim piśmiennictwie.
"Moglibyśmy całkowicie zahamować wzrostu guza po pojedynczej termoterapii mikrofalowej z użyciem ultra niskiej energii (1,8 W, 450 MHz) w modelu zwierzęcym", podsumowuje Meng. "Wierzymy, że ta nowatorska myśl otworzy nową erę w dziedzinie hipertermii nowotworowej."
Źródło: http://www.nanowerk.com/spotlight/spotid=40595.php
Tagi: nanotechnologia, platforma, termoterapia, nowotwor, rak
wstecz Podziel się ze znajomymi