- Biochemia
- Biofizyka
- Biologia
- Biologia molekularna
- Biotechnologia
- Chemia
- Chemia analityczna
- Chemia nieorganiczna
- Chemia fizyczna
- Chemia organiczna
- Diagnostyka medyczna
- Ekologia
- Farmakologia
- Fizyka
- Inżynieria środowiskowa
- Medycyna
- Mikrobiologia
- Technologia chemiczna
- Zarządzanie projektami
- Badania kliniczne i przedkliniczne
Starzenie się organizmu - nieunikniony skutek cyklu biologicznego
Streszczenie
Starzenie się jest procesem fizjologicznym o złożonej strukturze. Wszystkie organizmy żyjące na ziemi podlegają temu procesowi. Etap starości poprzedzony jest zmianami w organizmie, które zachodzą w komórkach, tkankach i organach w sposób nieuporządkowany. Duży wpływ na długość naszego życia ma aktywność fizyczna, sposób odżywiania się, środowisko, relacje społeczne czy rodzaj wykonywanej pracy.
Zjawisko starzenia jest wynikiem występowania sieci powiązanych ze sobą procesów. Gerontologia jest nauką, która w ostatnim stuleciu poszerzyła zasoby informacji, związane z procesem starzenia, o ponad sto teorii, które zostały potwierdzone bądź niepotwierdzone doświadczalnie. Teorie, które zostały rozpatrzone pozytywnie wciąż stanowią otwarte koncepcje, stale ulegające zmianom i uzupełnieniom. W poniższym artykule przeglądowym omówione zostały teorie próbujące wyjaśnić procesy starzenia takie jak teoria rodnikowa, telomerowa oraz teoria starzenia komórkowego.
Teoria rodnikowa i telomerowa
Jedną z teorii wyjaśniających zjawisko starzenia się jest teoria rodnikowa, mówiąca o wpływie wolnych rodników na procesy komórkowe. Twórcą tej teorii jest DENHAM HARMAN. Najważniejszymi związkami stanowiącymi podstawy życia organizmów są białka, lipidy i kwasy nukleinowej (DNA, RNA). HARMAN twierdzi, iż uszkodzenia zachodzące w makrocząsteczkach spowodowane są aktywnością wolnych rodników, czyli reaktywnych form tlenu (RFT) (HARMAN, 1956). Reakcje utleniania zachodzące w mitochondriach – głównych organellach odpowiedzialnych za proces oddychania – są źródłem tych cząsteczek. RFT powstają w wyniku wstrzymania procesu przyłączania elektronów do cząsteczki tlenu. Są one ubocznym produktem nie tylko reakcji utleniania, ale także promieniowania jonizującego (HARMAN, 1956; MICHALAK, 2014) czy działania ksenobiotyków – substancji egzogennych, szeroko występujących w przemyśle. Związki te obecne są w organizmie człowieka najczęściej w postaci leków bądź składników pożywienia. Ulegają one procesom modyfikacji oksydacyjnych, których wynikiem są uszkodzenia makromolekuł (PUZANOWSKA-TARASIEWICZ, 2008).
Pęknięcia nici kwasu dezoksyrybonukleinowego bądź transformacja zasad azotowych, to przekształcenia powstałe podczas wpływu RFT na cząsteczkę DNA (zarówno DNA jądrowe jak i mitochondrialne). W przypadku mutacji zachodzących w DNA mitochondrialnym (mtDNA) całe mitochondrialne DNA jest powielane i przekazywane komórkom potomnym w wadliwej formie. Wynika to ze struktury mtDNA. W przeciwieństwie do DNA jądrowego, nie zawiera ono odcinków niekodujących tzw. intronów (KULBACKA, 2009; MICHALAK, 2014; MIKUŁA-PIETRASIK, 2015).
Mutacje punktowe zachodzące w DNA spowodowane są występowaniem zjawisk takich jak substytucja (transwersja oraz tranzycja), insercja czy delecja (CHAMARY, 2009; SADAKIERSKA-CHUDY, 2004). Na przykład transwersja, czyli zamiana zasady purynowej na pirymidynową bądź odwrotnie, jest zjawiskiem uwarunkowanym obecnością zmodyfikowanych zasad azotowych np. 8-oksy-2'deoksyguanozyny. Mutacje powstałe w wyniku wyżej wymienionych procesów nie muszą dokonywać zmian w organizmie (tzw. mutacja cicha). Oznacza to, iż zmiana w sekwencji nukleotydów nie ma wpływu na funkcjonowanie genomu. W przypadku, gdy zamiana zasady azotowej powoduje powstanie innego aminokwasu niż był w pierwotnej wersji kodowanego białka, następuje zmiana struktury kodowanego polipeptydu. Nowo powstałe białko ingeruje w proces proliferacji komórek, co może być punktem wyjścia do procesu nowotworzenia (CHAMARY, 2009).
Zmiany na poziomie DNA skutkować mogą procesem skracania telomerów. Telomery są to odcinki materiału genetycznego stanowiące końcowe fragmenty chromosomów, których podstawową funkcją jest zapobieganie skracaniu chromosomu podczas replikacji. Z czasem telomery stają się krótsze w wyniku wielokrotnych replikacji DNA bądź RNA. Sekwencje telomerowe nie są już w żaden sposób chronione, więc komórka otrzymuje sygnał konieczności wyjścia z cyklu podziałowego. Proces podziałów komórkowych zostaje zatrzymany, a komórka umiera (OSTERHAGE, FRIEDMAN, 2009; KAZANOWSKA, 2003; BRYŚ, 2012).
Badania nad strukturą telomerów prowadzone są od bardzo dawna i nadal nie są poznane wszystkie ich funkcje. Osobami, które nazwały struktury chroniące chromosomy przed uszkodzeniami byli Herman Muller oraz Barbara McClintock (SIKORA, 2010). W roku 2009 naukowcy z USA Elizabeth H. Blackburn, Jack W. Szostak oraz Carol W. Greiner otrzymali Nagrodę Nobla z dziedziny Fizjologii i Medycyny (LIPIŃSKA, 2015). Naukowcy ci odkryli sposób w jaki telomery ochraniają chromosomy. Badania wykazały, iż telomery zachowują swoją strukturę i funkcje mimo zmian ewolucyjnych. Telomery nie były jednak jedynym obiektem ich badań. Dzięki badaniom biochemicznym wykryli oni enzym telomerazę. Telomeraza funkcjonuje w komórkach niepodlegających procesowi starzenia replikacyjnego i zapobiega skracaniu się telomerów (SIKORA, 2010; SIKORA, 2014; LIPIŃSKA, 2015).
Telomeraza to odwrotna transkryptaza tzn. polimeraza DNA zależna od RNA. Podjednostka TERC (ang. Telomerase RNA component) stanowi część enzymu, dzięki której możliwe jest wydłużanie telomerów, które ulegają skróceniu po każdym podziale (BRYŚ, 2012). Aktywność telomerazy zmienia się wraz z rodzajem komórki, np. telomery komórek rozrodczych nie skracają się co oznacza, że w tych komórkach aktywność telomerazy jest bardzo wysoka (KOWALSKA, 2006). W przypadku komórek macierzystych aktywność telomerazy również pozostaje na bardzo wysokim poziomie, choć dostrzegalny jest niewielki spadek liczby podziałów, a co za tym idzie starzenie komórek. Prawidłowe komórki somatyczne bardzo szybko skracają swoje telomery. Gdy długość telomerów osiągnie poziom krytyczny mogą one przekształcić się w komórki nowotworowe, które stabilizują długość telomerów. Jest to możliwe dzięki aktywacji telomerazy (MOON I JARSTWER, 2007).
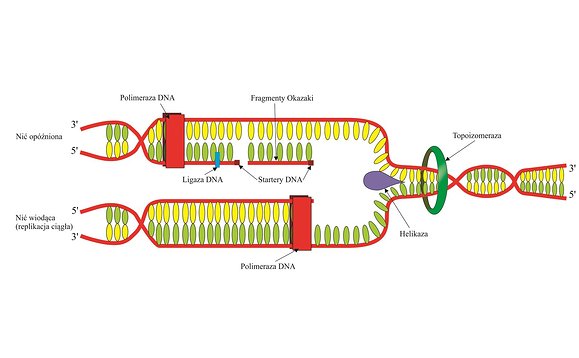
Rys. 1. Proces replikacji DNA
wstecz Podziel się ze znajomymi









Recenzje