- Biochemia
- Biofizyka
- Biologia
- Biologia molekularna
- Biotechnologia
- Chemia
- Chemia analityczna
- Chemia nieorganiczna
- Chemia fizyczna
- Chemia organiczna
- Diagnostyka medyczna
- Ekologia
- Farmakologia
- Fizyka
- Inżynieria środowiskowa
- Medycyna
- Mikrobiologia
- Technologia chemiczna
- Zarządzanie projektami
- Badania kliniczne i przedkliniczne
Przeciwciała poli- i monoklonalne - zastosowanie w medycynie
Szybki rozwój biotechnologii umożliwił otrzymywanie innych typów przeciwciał, tj. przeciwciał połączonych ze związkami chemicznymi, dzięki czemu możliwe jest poszerzenie zarówno właściwości tych związków, jak i ich zastosowań [10].
Przeciwciała mogą występować w postaci immunokoniugatów, tj. połączeń typu np. lek-przeciwciało lub lek-przeciwciało-biopolimer. Tego typu połączenie wpływa na zwiększenie stężenia leku, jakie może być dostarczane do komórek (np. komórek nowotworowych w trakcie terapii).
Znana jest również tzw. strategia ADEPT (ang. antibody-directed enzyme prodrug therapy), która wykorzystuje przeciwciało do przenoszenia enzymów, dzięki którym lek uwalniany jest z nieaktywnych proleków [4]. Dzięki lokalnemu działaniu (tylko w miejscu gromadzenia się przeciwciał) możliwe jest zmniejszenie toksyczności zastosowanej terapii [8].
Połączenie przeciwciał monoklonalnych z odpowiednimi cząsteczkami znalazły zastosowanie w medycynie klinicznej (immunohistochemia, Western Blotting, cytometria przepływowa) [1].
Komórki przeciwciał monoklonalnych mogą być modyfikowane, dzięki czemu wzmacnia się ich funkcje efektorowe. Można również zmodyfikować ich właściwości.Zdjęcie: Przeciwciała monoklonalne w terapii przeciwnowotworowej, [4].
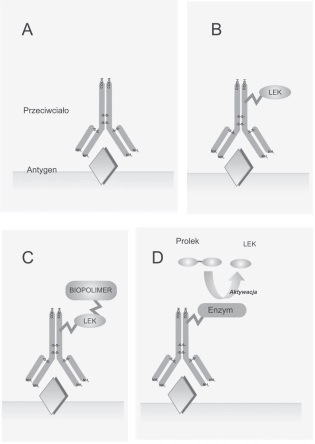
Opis do zdjęcia:
A. Przeciwciało monoklonalne;
B. Bezpośrednie przyłączenie leku do przeciwciała;
C. Zastosowanie biopolimeru, jako nośnika dla leku w immunokoniugacie;
D. Enzym, będący składnikiem koniugatu przekształca prolek w jego aktywną formę – terapia ADEPT[4].
Cząsteczka przeciwciała zawiera kilka potencjalnych miejsc, które biorą udział w reakcji koniugacji. Wśród nich wymienia się grupę ε – tj. aminową resztę lizyny. Reszta NH2 lizyny tworzy wiązanie amidowe z pochodnymi karbodiimidowymi. Dzięki temu do koniugatu mogą zostać wprowadzone grupy tiolowe, do których następnie przyłączane są leki. Niestety, jak wykazały przeprowadzane doświadczenia, zbyt duża liczba modyfikacji grup ε – aminowych lizyny może prowadzić do zmian właściwości immunoglobuliny, co oczywiście jest niepożądane. Dodatkowo modyfikacje w obrębie lizyny mogą prowadzić do neutralizacji ładunku dodatniego, co z kolei wpływa na zmianę rozpuszczalności danego przeciwciała. Drugim ze znanych sposobów otrzymywania koniugatów jest wprowadzanie reszty cukrowej w rejonie tzw. zawiasa przeciwciała. Miejsce to określane jest, jako fragment niezwiązany z miejscem wiążącym antygen. Opisana modyfikacja jest bezpieczna i nie wpływa na zmianę swoistości wiązania typu antygen – przeciwciało. Lek może zostać dołączony również do mostka disulfidowego, który występuje w cząsteczce przeciwciała. Mostek disulfidowy odpowiada za zachowanie stabilnej struktury immunoglobuliny, a przyłączenie leku do mostka disufidowego nie wpływa na swoistość przeciwciała [4].
Tagi: przeciwciała monoklonalne, przeciwciała poliklonalne, limfocyty B, komórka szpiczaka, komórki hybrydomy, reakcja koniugacji, immunokoniugaty, immunotoksyny, znakowanie przeciwciał, barwienie, kompleks przeciwciało-antygen
wstecz Podziel się ze znajomymi









Recenzje