- Biochemia
- Biofizyka
- Biologia
- Biologia molekularna
- Biotechnologia
- Chemia
- Chemia analityczna
- Chemia nieorganiczna
- Chemia fizyczna
- Chemia organiczna
- Diagnostyka medyczna
- Ekologia
- Farmakologia
- Fizyka
- Inżynieria środowiskowa
- Medycyna
- Mikrobiologia
- Technologia chemiczna
- Zarządzanie projektami
- Badania kliniczne i przedkliniczne
Wybrane metody wykorzystywane do oceny funkcji płytek krwi
W 1882 roku Giulio Bizzozero roku odkrył płytki krwi, nadając im status trzeciego elementu morfologicznego krwi. Wtedy też wyjaśniono funkcję tych komórek w hemostazie i zakrzepicy. Przez długi czas, płytek krwi i ich zawartość (granulaty) uważano głównie za komórki pośredniczące w aktywacji układu krzepnięcia. Z czasem odkryto wiele innych, ważnych ich funkcji [5].
Płytki krwi są komórkami, które pojawiają się w miejscu uszkodzenia tkanek. Komórki te wydzielają chemokiny, które aktywnie oddziałują na leukocyty (mobilizują je i kierują do miejsca zapalenia). Co więcej same również uczestniczą w procesach gojenia, a także wydzielają substancje bezpośrednio niszczące i uszkadzające bakterie (np. reaktywne formy tlenu). Tak, więc płytki krwi są ważnym elementem hemostazy, zapalenia i gojenia się ran [1].
Płytki krwi (PK) zaliczane są do najmniejszych, niemających jąder elementów morfotycznych krwi obwodowej i szpiku. Ich prawidłowa forma ma kształt dyskoidalny. Czas życia płytek krwi to od 8 do 12 dni, po czym komórki usuwane są z krwioobiegu przez układ siateczkowo-śródbłonkowy. Około 30% całkowitej masy płytek krwi występuje w śledzionie, gdzie stanowią tzw. pulę wymienialną [3].
Płytki krwi są reaktywnymi komórkami, które reagują na bardzo małe ilości krążących molekuł poprzez sekrecję aktywnych związków, które zmagazynowane są w ich ziarnistościach [4].
Wśród głównych funkcji płytek wymienia się ich udział w procesie hemostazy. Komórki, które znajdują się w krwiobiegu nie przylegają do śródbłonka wyścielającego ścianę naczynia krwionośnego, zaś przerwanie jego ciągłości i odsłonięcie warstwy podśródbłonkowej powoduje adhezję płytek krwi. Proces adhezji aktywuje przemiany płytek, na czele z syntezą tromboksanu A2 i sekrecją związków o określonej aktywności biologicznej oraz zmianą struktury receptora integrynowego αIIbβ2 napowierzchni, który może łączyć się np. z fibrynogenem [2]. Fibrynogen (osoczowy, jak i ten uwalniany z ziarnistości płytek) ma zdolność łączenia się z receptorami integrynowymi sąsiadujących płytek, dzięki czemu powstają agregaty płytkowe. Trombospondyna, która uwalniana jest z płytek ma za zadanie stabilizowanie wiązanego do płytek fibrynogenu i umacnianie powstających agregatów. Powstały dzięki szeregu reakcji hemostatyczny czop może uszczelniać drobne uszkodzenia powstałe w ścianie naczynia [2].
Trombospondyny (TSP) zaliczane są do rodziny białek wydzielniczych, które biorąc udział w oddziaływaniach między komórkami, a także między komórkami a macierzą zewnątrzkomórkową [8]. Białka te biorą udział w regulacji proliferacji, migracji i apoptozie komórek zarówno w warunkach fizjologicznych, jak i niektórych stanach patologicznych [9].
Najwcześniej odkrytym przedstawicielem tej rodziny białek jest trombospondyna-1 (TSP-1). W końcu lat 70-tych Lawer i wsp. odkryli, że białko to jest homotrimerem o masie cząsteczkowej 420 kDa, które uwalniane jest w odpowiedzi na trombinę. Gen tsp-1 kodujący białko trombospondynę-1 (TSP-1) zlokalizowano na krótszym ramieniu chromosomu 15 (15q15). TSP-1 produkowane jest przez wiele typów komórek m.in. przez płytki krwi, osteocyty, czy komórki nabłonka i śródbłonka [9].
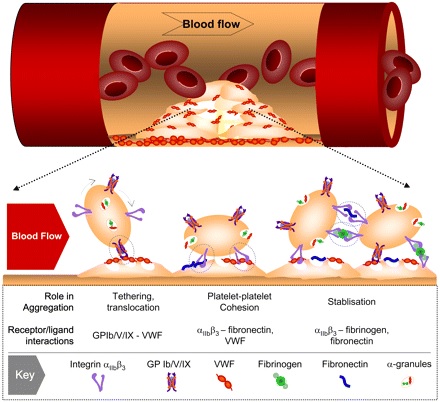
Zdjęcie: Proces agregacji płytek: stopniowe tworzenie się agregatów płytkowych i związki uczestniczące w procesie, http://www.bloodjournal.org/content/109/12/5087?sso-checked=true
Dzięki wysoce rozwiniętemu systemowi receptorów na błonie, płytki krwi wykazują zdolność reagowania na różnorodne bodźce, ulegają aktywacji i spełniają swoją określoną rolę w hemostazie. Receptory, które biorą udział w aktywacji płytek charakteryzują się zarówno różną budową, jak i mechanizmem działania [12]. Czynnikiem wywołującym adhezję i agregację płytek jest adenozynodifosforan (ADP) pochodzący z erytrocytów. Bardzo duże znaczenie w badaniach aktywacji płytek krwi indukowanej ADP miały pionierskie prace Born’a (prowadzone w latach 60-tych), a szczególnie wprowadzenie turbidymetrycznej metody badania agregacji i zmiany kształtu płytek [12].
Receptory płytkowe dla nukleotydu ADP odgrywają kluczową rolę w procesach formowania się skrzepu i patogenezie naczyniowej. Na powierzchni błony płytek krwi obecne są trzy typy receptorów: P2Y1 , P2Y12 oraz P2X. Receptory P2Y działają za pośrednictwem dwóch białek G, dzięki czemu aktywowane są wtórne przekaźniki wewnątrzkomórkowe. P2Y1 odpowiada za zapoczątkowanie procesu agregacji płytek poprzez mobilizację zasobów wapnia. Receptor P2Y12 poprzez hamowanie cyklazy adenylowej jest niezbędny dla pełnej odpowiedzi agregacyjnej. Z kolei receptor P2X jest kanałem jonowym o dużej szybkości przekazu, a jego udział w procesie pobudzania płytek krwi nie jest jeszcze do końca wyjaśniony [11], [15].









Recenzje